
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Última modificação 2025-01-22 17:07.
T / F como o visível espectro , um espectro de emissão atômica é um gama contínua de cores . T / F Cada elemento tem um único espectro de emissão atômica . T / F O fato de que apenas certo cores aparece em um elemento espectro de emissão atômica indica que apenas certas frequências de luz são emitido.
Tendo isso em mente, você poderia ver o comprimento de onda de um carro em movimento rápido?
Se tu olhou de perto, você poderia ver o comprimento de onda de um jejum - carro em movimento ? Você poderia não dizer, pois seria difícil se concentrar nas vibrações do carro . Usando a equação de de Broglie, λ = h / mv que teria um maior Comprimento de onda , tão baixo- em movimento próton ou um velozes - em movimento bola de golfe? Explique sua resposta.
Da mesma forma, por que os átomos emitem um espectro de linha definido de apenas certas energias em vez de um espectro contínuo de todas as energias? Há uma conexão íntima entre a estrutura atômica de um átomo e os seus espectral características. Átomos de elementos individuais emitir luz em apenas específico comprimentos de onda, produzindo um espectro de linha em vez de a espectro contínuo de todos comprimentos de onda produzidos por um objeto quente.
Além disso, o que é um questionário de espectro de emissão atômica?
Espectros de emissão atômica . A linha descontínua espectro de luz produzida quando excitado átomos retornam ao seu estado fundamental e emitem fótons de uma certa freqüência. Atômico Absorção Espectro . o espectro de certos comprimentos de onda de luz absorvidos correspondentes a um espectro do átomo do emitido frequências de luz.
Os orbitais atômicos têm um tamanho exatamente definido?
orbitais atômicos ( Faz , Faz não) tem um tamanho exatamente definido . Cada orbital pode conter no máximo (dois, quatro) elétrons. todos s orbitais são (formato esférico, formato de haltere). o número máximo de (elétrons, orbitais ) relacionado a cada nível de energia principal é igual a 2n ^ 2.
Recomendado:
O que causa as linhas no espectro de emissão dos elementos?

As linhas de emissão ocorrem quando os elétrons de um átomo, elemento ou molécula excitado se movem entre níveis de energia, retornando ao estado fundamental. As linhas espectrais de um elemento ou molécula específica em repouso em um laboratório sempre ocorrem nos mesmos comprimentos de onda
O que causa o espectro de emissão de um elemento?

Os espectros de emissão atômica surgem da queda de elétrons de níveis de energia mais altos para níveis de energia mais baixos dentro do átomo, fótons (pacotes de luz) com comprimentos de onda específicos são liberados
Como um espectro de emissão atômica é diferente de um espectro contínuo?

Espectro contínuo: um espectro que possui todos os comprimentos de onda sem intervalos em uma ampla faixa. Espectro de emissão: quando um elétron em um estado excitado se move para um nível de energia inferior, ele emite uma certa quantidade de energia na forma de fótons. O espectro para esta transição consiste em linhas porque os níveis de energia são quantizados
Por que o espectro de absorção da clorofila a e o espectro de ação da fotossíntese são diferentes?
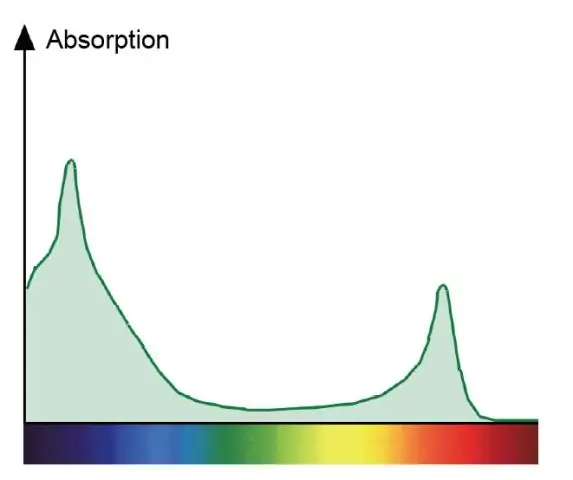
Um espectro de absorção mostra todas as cores da luz absorvida por uma planta. Um espectro de ação mostra todas as cores de luz que são usadas na fotossíntese. As clorofilas são os pigmentos verdes que absorvem o vermelho e o azul e participam da fotossíntese diretamente
Qual é o espectro de emissão do sol?

O espectro de emissão do sol. O Sol emite radiação eletromagnética em uma ampla faixa de comprimentos de onda. O máximo no espectro de emissão solar é de cerca de 500 nm, na parte azul-esverdeada do espectro visível. Assim como a luz visível, o Sol emite radiação ultravioleta e radiação infravermelha
