
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Última modificação 2025-01-22 17:08.
No ponto equivalente , quantidades iguais de H+ e OH- íons se combinarão para formar H2O, resultando em um pH de 7,0 (neutro). o pH no ponto de equivalência por esta titulação sempre será 7.0, observe que isso é verdadeiro apenas para titulações do ácido forte com base forte.
Em relação a isso, qual é o ponto de equivalência de um ácido forte e uma base fraca?
No ácido forte - titulações de base fraca , o pH no ponto equivalente não é 7, mas está abaixo dele. Isso se deve à produção de um conjugado ácido durante o titulação ; ele vai reagir com a água para produzir hidrônio (H3O+) íons.
Além disso, como você encontra o pH no ponto de equivalência? No caso de titulação de ácido fraco com base forte, pH no ponto equivalente é determinado pela hidrólise do sal de ácido fraco. Isso significa que temos que achar pKb de base conjugada e calcular concentração de OH- começando daí, então use pH = 14-pOH Fórmula.
Conseqüentemente, todas as titulações de uma base forte com um ácido forte têm o mesmo pH no ponto de equivalência?
Sim, toda base forte - titulações de ácido forte terminar com o mesmo PH porque o conjugado ácido e conjugado base são neutros. Sim, toda base forte - titulações de ácido forte terminar com o mesmo PH porque só resta água no copo quando a neutralização é concluída.
O que acontece quando um ácido forte reage com uma base forte?
Na verdade, quando um o ácido forte reage com uma base forte , os produtos resultantes são água e um sal iônico. Outro exemplo de tal reação é o químico reação entre o clorídrico ácido (HCl) e hidróxido de potássio (KOH).
Recomendado:
Você adiciona um ácido a uma base ou uma base a um ácido?

Adicionar um ácido aumenta a concentração de íons H3O + na solução. Adicionar uma base diminui a concentração de íons H3O + na solução. Um ácido e uma base são como opostos químicos. Se uma base é adicionada a uma solução ácida, a solução se torna menos ácida e se move em direção ao meio da escala de pH
Como você encontra a equação de uma linha perpendicular a um ponto?
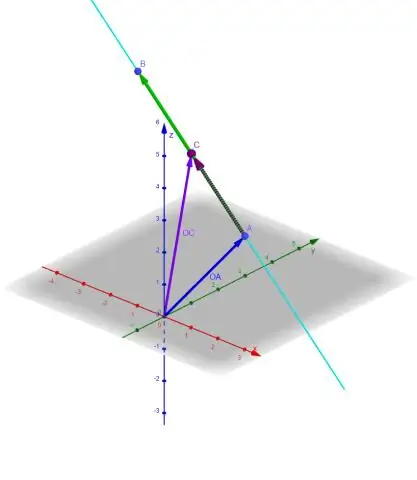
Primeiro, coloque a equação da linha dada na forma de interceptação da inclinação resolvendo por y. Você obtém y = 2x +5, então a inclinação é –2. As linhas perpendiculares têm inclinações opostas recíprocas, de modo que a inclinação da linha que queremos encontrar é 1/2. Conectando o ponto dado na equação y = 1 / 2x + be resolvendo para b, obtemos b = 6
Como você encontra a equação de uma linha dado um ponto e uma linha paralela?
A equação da reta na forma de interceptação em declive é y = 2x + 5. A inclinação da paralelina é a mesma: m = 2. Portanto, a equação da reta paralela é y = 2x + a. Para encontrar a, usamos o fato de que a linha deve passar pelo ponto dado: 5 = (2) ⋅ (− 3) + a
O que torna um ácido um ácido e uma base uma base?

Um ácido é uma substância que doa íons de hidrogênio. Por causa disso, quando um ácido é dissolvido na água, o equilíbrio entre os íons hidrogênio e os íons hidróxido é alterado. Esse tipo de solução é ácida. Uma base é uma substância que aceita íons de hidrogênio
O que aconteceria se você misturasse um ácido forte com uma base igualmente forte?

O que aconteceria se você misturasse um ácido forte com uma base igualmente forte? Você veria uma reação química explosiva. O ácido destruiria a base. A base iria destruir o ácido
