
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Última modificação 2025-01-22 17:07.
A presença de apenas algumas linhas no atômico espectro significava que um elétron só pode adotar certos níveis de energia discretos (a energia é quantizada); daí a ideia de quantum cartuchos . As frequências de fótons absorvidas ou emitido por um átomo são fixados pelas diferenças entre os níveis de energia das órbitas.
Com relação a isso, como o modelo de Bohr contabiliza os espectros de emissão dos átomos?
Modelo de Bohr do hidrogênio átomo deu uma explicação exata para sua observação Espectro de emissão . Os elétrons podem se mover de uma órbita para outra absorvendo ou emitindo energia, dando origem a características espectro.
que evidências apóiam o modelo de Bohr? Modelo Bohr e espectros atômicos evidência costumava ser apoiar o modelo Bohr veio dos espectros atômicos. Bohr sugeriu que um espectro atômico é criado quando os elétrons em um átomo se movem entre níveis de energia.
A respeito disso, que evidência existe de elétrons em camadas?
Energia de ionização - a evidência para cartuchos e sub- cartuchos Energia de ionização é uma medida de a quantidade de energia necessária para remover elétrons dos átomos. Como elétrons são carregados negativamente e prótons em a núcleos são carregados positivamente, lá será uma atração entre eles.
Como você encontra o espectro de emissão?
As frequências de luz que um átomo pode emitir dependem dos estados em que os elétrons podem estar. Quando excitado, um elétron se move para um nível de energia ou orbital mais alto. Quando o elétron volta ao nível do solo, a luz é emitido.
Recomendado:
Quais são as camadas de elétrons de um átomo?

Uma camada de elétrons é a parte externa de um átomo ao redor do núcleo atômico. É onde estão os elétrons, e é um grupo de orbitais atômicos com o mesmo valor do número quântico principal n
Por que o modelo de Bohr pode ser chamado de modelo planetário do átomo?

O motivo pelo qual é chamado de "modelo planetário" é que os elétrons se movem ao redor do núcleo de maneira muito semelhante aos planetas que se movem ao redor do sol (exceto que os planetas são mantidos perto do sol pela gravidade, enquanto os elétrons são mantidos perto do núcleo por algo chamado uma força de Coulomb)
Como os espectros de emissão são evidências para camadas de elétrons?

A presença de apenas certas linhas no espectro atômico significa que um elétron só pode adotar certos níveis de energia discretos (a energia é quantizada); daí a ideia de conchas quânticas. As frequências de fótons absorvidas ou emitidas por um átomo são fixadas pelas diferenças entre os níveis de energia das órbitas
Como Niels Bohr descreve os elétrons em seu modelo atômico?
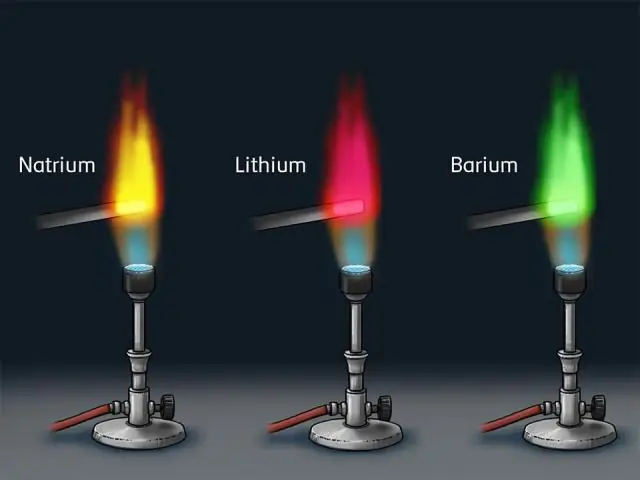
Modelo Atômico de Bohr: Em 1913, Bohr propôs seu modelo de camada quantizada do átomo para explicar como os elétrons podem ter órbitas estáveis ao redor do núcleo. A energia de um elétron depende do tamanho da órbita e é menor para órbitas menores. A radiação pode ocorrer apenas quando o elétron salta de uma órbita para outra
Como o modelo de Bohr explica os espectros atômicos?

Niels Bohr explicou o espectro de linha do átomo de hidrogênio assumindo que o elétron se movia em órbitas circulares e que órbitas com apenas certos raios eram permitidas. A órbita mais próxima do núcleo representava o estado fundamental do átomo e era mais estável; órbitas mais distantes eram estados excitados de alta energia
